화학에서 같은 주기에서 원자번호가 증가할 때 이온 반경이 어떻게 변하는지는
주기율표와 전자배치의 이해와 관련이 깊어요.

✅ 결론부터 말하면:
같은 주기에서는 원자번호가 증가할수록 이온 반경은 작아집니다.
💡 왜 그런가요?
1. 같은 주기란?
- 같은 주기 = **같은 전자껍질(에너지 준위)**을 가진 원소들이에요.
- 예: 2주기 → Li, Be, B, C, N, O, F, Ne
2. 원자번호 증가 → 양성자 수 증가
- 핵의 양성자 수가 많아질수록 전자들을 더 세게 끌어당기게 돼요.
- 전자가 같은 껍질에 있어도 전자 구름이 더 조여져서 작아짐 👉 반지름 작아짐
3. 이온 반경은 어떻게 적용돼요?
✅ 양이온(+):
- 전자를 잃으면서 전자껍질 수가 줄거나, 전자 간 반발이 줄어들어 작아짐
- 예: Na⁺ < Mg²⁺ < Al³⁺ → 이온 반경이 점점 작아짐
✅ 음이온(−):
- 전자를 얻으면 전자 간 반발이 커지며 부피 증가
- 예: N³⁻ > O²⁻ > F⁻ → 음이온이라도 원자번호가 클수록 반경은 작아짐
📌 요약 정리
| 같은 주기 내 | 전자껍질 수 동일 |
| 원자번호 증가 | 핵전하↑ → 전자당김↑ |
| 이온 반경 | 점점 작아짐 |
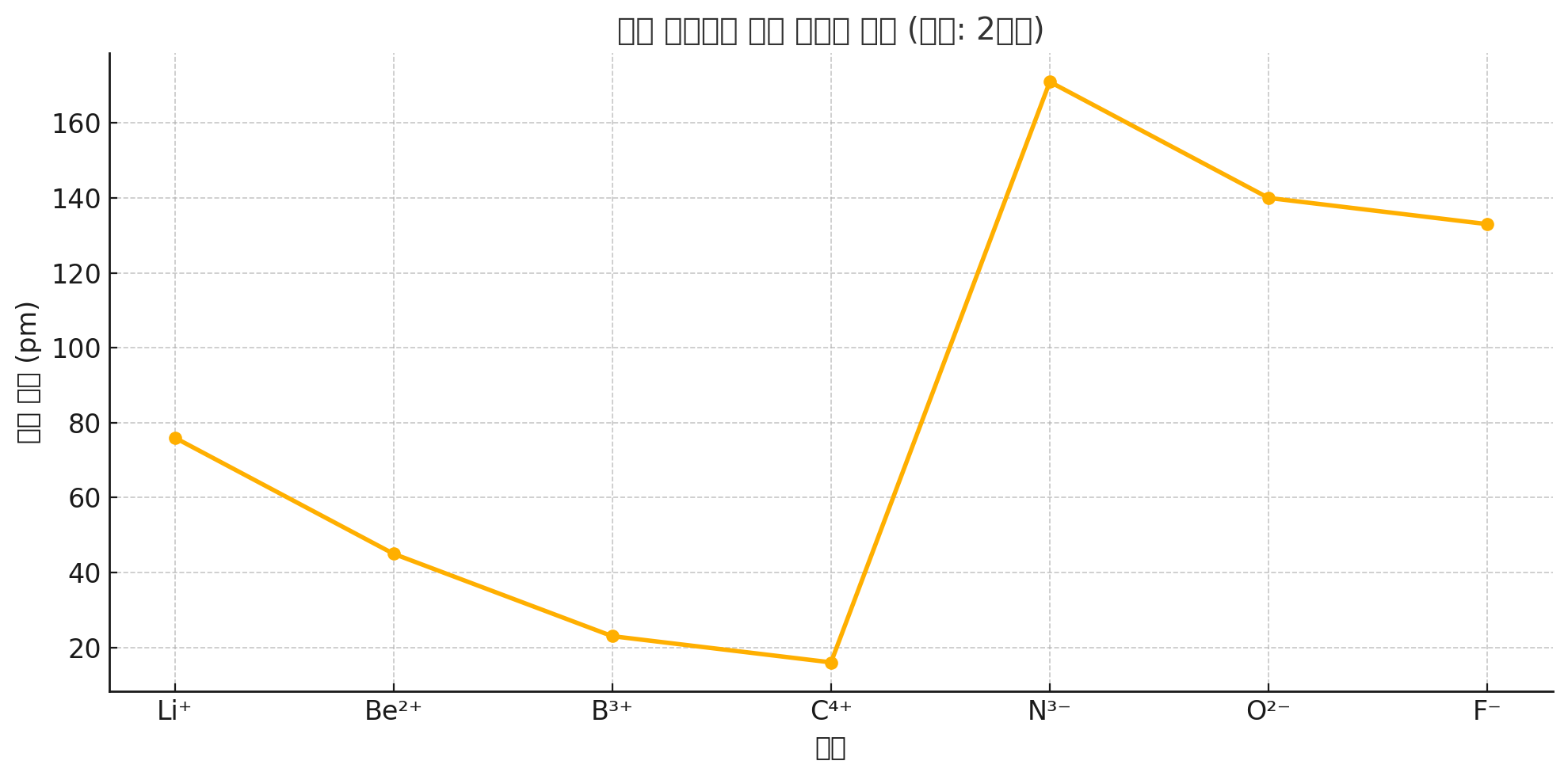
여기 그래프를 보시면, 같은 2주기 원소들이 이온이 되었을 때의 반지름 변화를 나타냅니다.
- 왼쪽(Li⁺, Be²⁺, B³⁺) 쪽은 양이온 → 전자 수 감소 → 반경 작아짐
- 오른쪽(N³⁻, O²⁻, F⁻) 쪽은 음이온 → 전자 수 증가 → 반경 커짐
- 전체적으로 보면, 같은 주기 안에서 원자번호가 증가할수록 이온 반경은 작아지는 경향이 뚜렷하게 나타나죠!
📌 즉, 핵전하가 커질수록 전자들을 더 강하게 끌어당기게 되어, 같은 껍질이라도 이온 반경은 작아지는 거예요.
[공부블로그]토익 RC 같이 공부해요
오늘은 지난번 LC같이 풀기에서 말씀드렸던 토익 RC 풀기를 해볼거에요 제가 공부하는 문제집은 지난번 LC문제집과 동일한 책 RC버전이에요 10회짜리라서 꽤 두꺼워요. (무거우니까 인터넷 배송
lepoales.tistory.com
구리와 크롬의 전자배치
구리(Cu)와 크롬(Cr)의 전자배치는 일반적인 규칙에서 예외적으로 나타나는 대표적인 원소들입니다. 각각의 전자배치는 다음과 같습니다:✅ 크롬 (Cr, 원자번호 24)기본 규칙대로라면:1s² 2s² 2p⁶ 3
studywithnal.com
[공부블로그]토익 LC 같이 공부해요
오늘은 토익 LC를 공부했어요 듣기는 점수가 잘 나오더라도 꾸준히 해주어야 좋을 것같아요. 아무래도 모국어가 아니기 때문에 안듣는 텀을 너무 길게 갖으면 감을 잃더라구요 ㅠㅠ 토익 고득점
lepoales.tistory.com
'공부내용' 카테고리의 다른 글
| TCA 회로란? (1) | 2025.04.09 |
|---|---|
| 🔬 처음 배우는 화학 개념: 이온화 에너지 vs 전자친화도 (0) | 2025.04.09 |
| 💊 약대 편입, 어떻게 준비해야 할까요? (0) | 2025.04.08 |
| 당신생합성(glycogenesis) (1) | 2025.04.08 |
| 구리와 크롬의 전자배치 (0) | 2025.04.08 |


